¿Qué es la
saponificación?
La saponificación es
un proceso químico por el cual un cuerpo graso, unido a
un álcali y agua, da como resultado jabón y glicerina. Se llama
jabones a las sales sódicas y potásicas derivadas de los ácidos grasos. Son
susceptibles de saponificación todas aquellas sustancias que en su estructura
molecular contienen restos de ácidos grasos, y son sustancias naturales a las
que llamamos lípidos saponificables.

¿cuales son los lípidos saponificables más abundantes ?
Los lípidos saponificables más abundantes en la naturaleza
son las grasas neutras o glicéridos. La saponificación de
un triglicérido se resume así:
grasa + sosa
cáustica → jabón + glicerina.
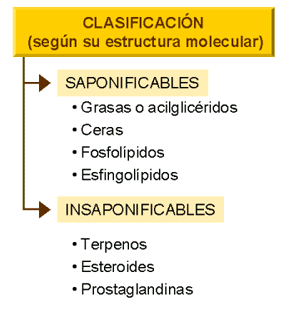
Tipos de lípidos por
sus características de Saponificación
Un lípido
saponificable es
aquel que esté
compuesto por un alcohol unido a uno o varios ácidos grasos. Esta unión se realiza
mediante un enlace éster, muy difícil de hidrolizar. Pero puede
romperse fácilmente si el lípido se encuentra en un medio básico. En
este caso se produce la saponificación alcalina. En los casos en los que para
la obtención del jabón se utiliza un glicérido o grasa neutra, se
obtiene como subproducto el alcohol llamado glicerina.
Lograr la
transparencia del jabón.
Un exceso de ácidos grasos en el jabón hace que éste sea
opaco y de consistencia lechosa.
Cuando se hace un jabón mediante un procedimiento en frío,
el jabón saldrá opaco, aunque hayamos sido muy precisos en la medida
de álcalis y aceites, ya que este proceso rara vez produce
el calor suficiente para neutralizar por completo
los ácidos grasos.
¿& Cuando el
proceso es caliente?
El proceso en caliente incorpora el calor de
la cocina al calor químico producido por la saponificación. Este calor añadido
une todos los ácidos grasos con el álcali y como resultado tenemos un jabón
transparente y neutro.
La saponificación es una reacción química que produce
calor, y cuanto más calor produzca más completa será la saponificación.
tablas de
saponificación.
Sustancia
|
Índice de saponificación
|
Sustancia
|
Índice de saponificación
|
Aceite de oliva
|
0,134
|
Aceite de coco
|
0,190
|
Aceite de palma
|
0,141
|
Aceite de girasol
|
0,134
|
Aceite de ricino
|
0,128
|
Aceite de Almendras Dulces
|
0,136
|
Aceite de aguacate
|
0,133
|
Aceite de soja
|
0,135
|
Aceite de maíz
|
0,136
|
Aceite de sésamo
|
0,133
|
Aceite de jojoba
|
0,069
|
Aceite de palmiste
|
0,156
|
Aceite de germen de
trigo
|
0,132
|
Cera de abeja
|
0,069
|
Elaboración
en laboratorio
Con aceite:
Disolver las perlas de hidróxido de sodio NaOH(sol), para ello pesamos 20 gr de NaOH en la balanza, transferimos el
contenido a un matrás aforado de 100 ml y enrasamos con agua
destilada para obtener una disolución al 20 %.
Colocar 100ml de aceite en un recipiente, y lo mezclamos con la
disolución de hidróxido de sodio.
Calentar durante 30 min. aproximadamente, al baño maría con
cuidado.
Dejar reposar durante 24 h a temperatura ambiente, para que se
forme el jabón.
Con grasa animal:
Disolver las perlas de hidróxido para obtener una disolución al
20 %.
Pesar 100 gr de grasa animal en la balanza.
Calentar al baño maría porque se encuentra en estado semisólido
debe estar más fluida.
Luego mezclar con la disolución de hidróxido de sodio y de nuevo
calentar la mezcla al baño maría con cuidado.
Dejar reposar para ver los resultados.
Función de cada elemento
La SODA CAUSTICA o Hidróxido de Sodio (NaOH) reacciona
químicamente con una amplia variedad de químicos orgánicos e inorgánicos. En
todas sus formas, incluyendo en solución, la soda cáustica es muy corrosiva y
puede causar quemaduras serias a los ojos y la piel. El contacto con los ojos
de sólo unos pocos segundos puede acusar daño permanente, aún la ceguera.
Incluso un contacto de corta duración con la piel puede causar intensa
irritación o quemaduras de tipo químico.
Reactividad y estabilidad
Estabilidad: El producto absorbe agua y dióxido de
carbono del aire. Se debe de mantener los recipientes cerrados y sellados.
Condiciones que deben evitarse: Puede reaccionar
violentamente con agua, ácidos y compuestos orgánicos. Puede generar hidrógeno
cuando entra en contacto con metales como estaño, aluminio, zinc y bronce. El
hidrógeno es inflamable y explosivo.
Incompatibilidad con otras sustancias: Agua y ácidos.
Manejo y almacenamiento
Manejo: Se debe de evite el contacto con los ojos o la
piel. No respire sus polvos.
Almacenamiento: Evite almacenar el producto cerca de
ácidos fuertes. La soda cáustica debe almacenarse en áreas secas y limpias. No
almacene en tanques subterráneos
Identificación de riesgos
°Ojos: Puede
causar irritación severa con daño a la córnea y resultar en un deterioro
permanente de la visión, causando hasta la ceguera.
°Piel: Breves
exposiciones pueden causar severas quemaduras en la piel. Es un producto
clasificado como corrosivo.
°Ingestión:
Puede causar irritación gastrointestinal o ulceraciones y quemaduras severas de
la boca y garganta.
°Inhalación:
Polvos y vaporizaciones del producto pueden causar irritaciones severas en la
parte superior del aparato respiratorio.
PRECAUCIONES DE SEGURIDAD Y
MEDIDAS PREVENTIVAS
La solución de soda cáustica es un químico industrial
muy corrosivo. No parece ser peligroso, tiene la apariencia de agua, pero el
contacto de tan sólo unos pocos segundos con los ojos puede causar daño
permanente, incluso la ceguera.
Como la soda cáustica es incolora, no se
advierte el peligro. Además, la soda cáustica no produce dolor inmediato cuando
entra en contacto con la piel, pero si causa daño inmediato. Un contacto de
corta duración con la piel, puede causar irritación intensa o quemadura de tipo
químico.
PRIMEROS AUXILIOS
En caso de contacto con soda cáustica enjuáguese con
agua solamente. No intente neutralizar la soda cáustica con productos químicos.
Continúe enjuagándose con agua durante media hora o siga las instrucciones del
médico. No vaya al hospital o a un centro médico puesto que éstos no podrán
suministrar otro tratamiento distinto al enjuague con agua y la pérdida de
tiempo durante el transporte de la víctima puede causar un daño irreparable.
°Ojos:
Enjuáguese inmediatamente con agua a baja presión en la fuente lavaojos. Una
vez que se haya enjuagado las manos completamente, mantenga los párpados
abiertos y continúe lavándose durante media hora.
°Cuerpo: Lávese
inmediatamente con agua en la ducha de seguridad. Lave la zona afectada con
agua durante media hora. Quítese la ropa mientras se ducha. Si los ojos no han
estado expuestos, no se quite los anteojos de seguridad hasta que se haya
enjuagado completamente la cabeza y el cabello, puesto que la soda cáustica
podría entrar a los ojos. Enjuáguese la cabeza completamente, quítese los
anteojos y siga lavándose.
°Ingestión
(tragar): No induzca el vómito. Suministre inmediatamente grandes cantidades de
leche (de preferencia) o agua y llame al médico.
°Manos:
enjuáguese con agua hasta que la sensación resbaladiza desaparezca.
°Ropas: Lave la
ropa contaminada para eliminar la soda cáustica, antes de volver a ponérsela.
Los zapatos contaminados y los artículos de cuero deben ser desechados.
MEDIDAS A TOMAR EN CASO DE
EMISIONES ACCIDENTALES
Evacue y ventile el área del derrame. Utilice equipo
de protección personal completo durante la limpieza.
Solamente el personal entrenado y protegido
adecuadamente puede involucrase en las operaciones de limpieza de derrame.
Conclusiones
• Se analizó la formulación para elaborar el producto,
teniendo en cuenta los conocimientos adquiridos en el área de química.
• Se elaboró un jabón con calidad, utilizando grasas
animales y esencias naturales aptas para su uso.
• Se analizó la composición de la soda caustica y su
peligrosidad al contacto directo, y que al ser mezclada con otros elementos son
aptos para el consumo en el hogar.
• Se observo la importancia de la química en las
diferentes aplicaciones en la vida cotidiana.
De la teoría a la practica.
De la teoría a la practica.
Materiales para el proceso de saponificación:
1- soda caustica
2- recipiente de pastico
3- un palote (para revolver)
4- aceite vegetal o animal
5- agua
6- aceite aromatizante
7- colorante
8- moldes
9- sal
10- estufa
Materiales para el cuidado personal durante el experimento:
1- tapabocas
2- bata de laboratorio
3- guantes
Procedimiento:
1- se midieron las proporciones de los ingredientes:
° soda caustica (250 gm)
° 1.5 litros de agua
° 1.5 litros de aceite
° sal al gusto
° colorante al gusto
° aceite aromático
2- se vacía la soda caustica al recipiente de plástico
3- se agrega agua al recipiente con la soda caustica, esta se
mezcla y se torna de color blanco desprendiendo un aire caliente, se revuelve
constantemente hasta que esta se torna transparente.
4- se coloca a tibiar el aceite, una vez tibio se agrega a la
mezcla de agua y soda caustica, se sigue revolviendo constantemente durante 20
minutos, Tomando esta un tomo amarillo opaco.
5- una vez obtenida la
mezcla de tono amarillo se agrega el colorante y el aceite aromatizante
obteniendo un tono anaranjado-amarillo. Teniendo en cuenta que hay que estar
revolviendo constantemente.
6-se agrego la mezcla a los moldes de aluminio, pero como no era
recomendable tubo efectos secundarios y se tubo que volver a depositar en el
balde hasta que se reposara para poderlo echarlo en los moldes.
Extras






























Este comentario ha sido eliminado por el autor.
ResponderBorrarme encantan los resultados compañeros
ResponderBorrarsin duda alguna estos espacios nos permiten dejar volar toda nuestra creatividad en la ciencia y sobre todo en la quimica